Bezpečnostný profil
Bezpečnostný profil
Nasledujúce údaje odrážajú expozíciu lieku WINREVAIR® v kľúčovej štúdii STELLAR.
- Po ukončení primárnej 24-týždňovej fázy liečby pacienti pokračovali v dlhodobej dvojito zaslepenej liečbe (LTDB), pričom si zachovali svoju súčasnú liečbu, až kým všetci pacienti neukončili primárne obdobie liečby.
- Medián trvania liečby bol v skupinách s placebom a s liekom WINREVAIR® podobný (229,5 dní v porovnaní s 252,0 dňami).
Nežiaduce reakcie, ktoré sa vyskytli v štúdii STELLAR v čase, keď všetci pacienti ukončili primárne 24-týždňové obdobie štúdie, sú zhrnuté nižšie.
Nežiaduce reakcie u pacientov, ktorí dostávajú WINREVAIR® (DBPC + LTDB)a:
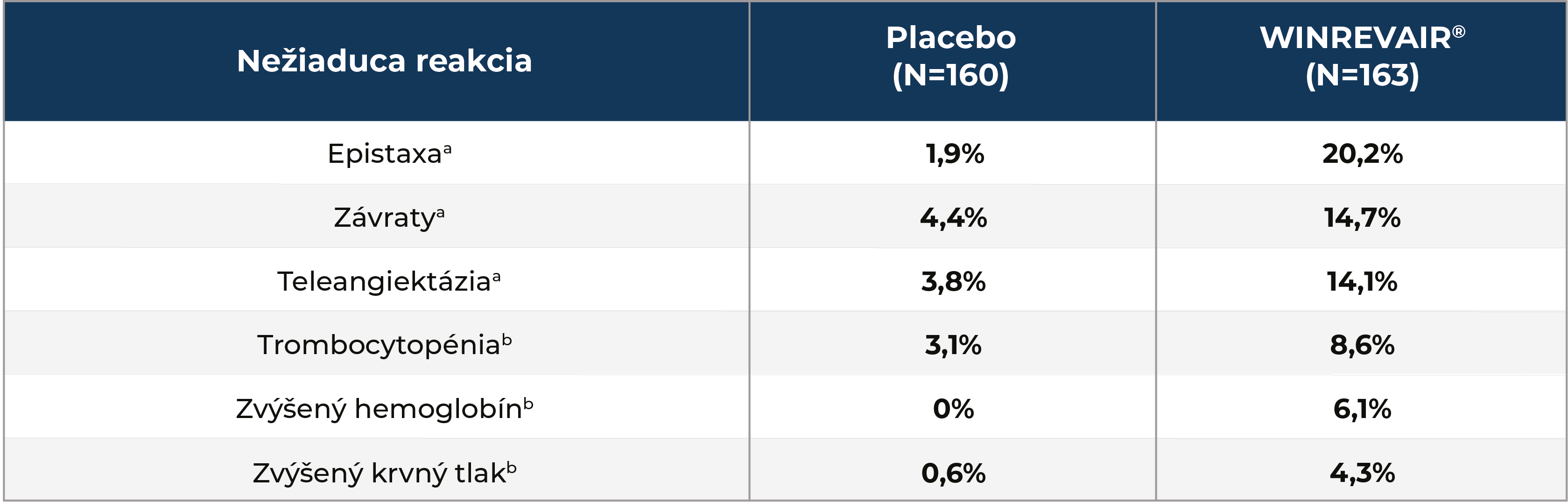
aDvojito zaslepené obdobie kontrolované placebom * dlhodobé dvojito zaslepené obdobie.
bKompozitné pojmy.
Zvýšený hemoglobín
Väčšina prípadov zvýšeného hemoglobínu (zvýšený Hgb, polycytémia) bola nezávažná, mierna a reverzibilná a nesúvisela s prerušením liečby.
- Stredne závažné zvýšenie Hgb (> 2 g/dl nad hornú hranicu normy [ULN]) sa vyskytlo u 15,3 % pacientov užívajúcich WINREVAIR®.
- Neboli pozorované žiadne závažné zvýšenia (≥ 4 g/dl nad ULN).
- Zvýšenie Hgb sa dalo zvládnuť blízkymi odkladmi, znížením dávky alebo oboma spôsobmi.
Trombocytopénia
Väčšina prípadov trombocytopénie (trombocytopénia a zníženie počtu trombocytov) bola nezávažná, mierna, reverzibilná a nesúvisela s prerušením liečby.
- Závažné zníženie počtu krvných doštičiek <50 000/mm3 (<50,0 x 109/l) sa vyskytlo u 2,5 % pacientov užívajúcich WINREVAIR®.
- Trombocytopénia sa vyskytla častejšie u pacientov, ktorí dostávali aj prostacyklínovú infúziu (21,5 % užívajúcich WINREVAIR® a 0 % užívajúcich placebo) v porovnaní s pacientmi, ktorí neužívali prostacyklínovú infúziu (3,1 % pacientov užívajúcich WINREVAIR® a 3,1 % pacientov užívajúcich placebo).
Teleangiektázia
Prípady teleangiektázie neboli závažné a ich závažnosť sa časom nezmenšovala.
- U všetkých pacientov, ktorí dostávali liek WINREVAIR® bol medián času do nástupu 18, 6 týždňa.
- Prerušenie liečby z dôvodu teleangiektázie sa vyskytlo u 1 % v skupine WINREVAIR® v porovnaní s 0 % v skupine s placebom.
- S teleangiektáziou neboli spojené žiadne prípady závažného krvácania.
Zvýšený krvný tlak
Prípady zvýšeného krvného tlaku (hypertenzia, zvýšený diastolický krvný tlak, zvýšený krvný tlak) neboli závažné a neboli hlásené žiadne závažné príhody.
- U pacientov užívajúcich WINREVAIR® sa priemerný systolický krvný tlak zvýšil v porovnaní s východiskovou hodnotou o 2,2 mmHg a diastolický krvný tlak sa zvýšil o 4,9 mmHg počas 24 týždňov.
- U pacientov užívajúcich placebo bola zmena priemerného systolického krvného tlaku v porovnaní s východiskovou hodnotou -1,6 mmHg a zmena diastolického krvného tlaku -0,6 mmHg.
Prerušenie liečby
Celkový výskyt prerušenia liečby z dôvodu nežiaducej reakcie bol 4 % v skupine WINREVAIR® a 7 % v skupine s placebom.
Nevyskytli sa žiadne špecifické nežiaduce reakcie, ktoré by spôsobili prerušenie liečby a ktoré by sa vyskytli s frekvenciou vyššou ako 1 % a častejšie v skupine WINREVAIR®.
Údaje o dlhodobej bezpečnosti
K dispozícii sú údaje o dlhodobej bezpečnosti z klinického skúšania fázy 2 (PULSAR), ktoré pozostávalo z 24-týždňového, dvojito zaslepeného, placebom kontrolovaného obdobia liečby, po ktorom nasledovalo 30-mesačné, otvorené predĺžené obdobie (n=104). Väčšina z týchto pacientov potom pokračovala v dlhodobej následnej štúdii.
- Priemerné trvanie expozície lieku WINREVAIR® v štúdii PULSAR a v dlhodobej následnej štúdii bolo 151 týždňov s maximálnou expozíciou 218 týždňov.
- Bezpečnostný profil bol vo všeobecnosti podobný profilu pozorovanému v kľúčovej štúdii STELLAR.
-
Teleangiektázia sa však počas dvojito zaslepenej, placebom kontrolovanej liečby v štúdii PULSAR nepozorovala.
- Teleangiektázia bola prvýkrát hlásená v otvorenom predĺžení, pričom sa po ukončení štúdie vyskytla u 27 % pacientov s mediánom času do nástupu 106 týždňov.
